《Cell》:乳腺癌类器官生物样本库重现了疾病的异质性
生 物 智 造 创 建 美 好 生 活
Intelligent Biomanufacturing Creates Better Life
乳腺癌(BC)是全世界妇女中最常被诊断的癌症和癌症死亡的原因。乳腺癌包括20多种不同的亚型,在遗传学、形态学和临床上都有差异。下一代测序通过绘制BC分子画像和对BC基因中多个驱动突变的发现验证了BC的异质性。目前的标准系统疗法(激素、细胞毒性和HER2靶向)并不能实现个体化治疗。来自Hubrecht Institute 的Hans Clevers团队的Norman Sachs等建立了人类乳腺上皮细胞类器官培养方法,基于此成功构建100多个原发性和转移性BC类器官,再现了该疾病的多样性。BC类器官的形态通常与原始肿瘤的组织病理学、激素受体状态和HER2状态相匹配。肿瘤和配对的类器官中的DNA拷贝数以及序列变化是一致的,在多次传代后也是如此。这项研究报道了一个可用于癌症研究和药物开发的、分类明确的BC类器官样本库,以及一个以个性化方式评估体外药物反应的策略。
01
建立BC类器官生物样本库
分离出的细胞采用BME水凝胶包裹,并采用优化的BC类器官培养基培养(图1A)。类器官的成功构建未显示受到原始BC的组织学亚型、分级或受体状态影响(图1B)。作者观察到不同大小的固体类器官、囊性类器官、"葡萄状 "类器官和几乎完全不粘连的类器官(图1C)。为了生成一个注释完备的生物样本库,作者通过组织学、WGS、RNA-seq和药物测试(图1D)来深入分析BC类器官。
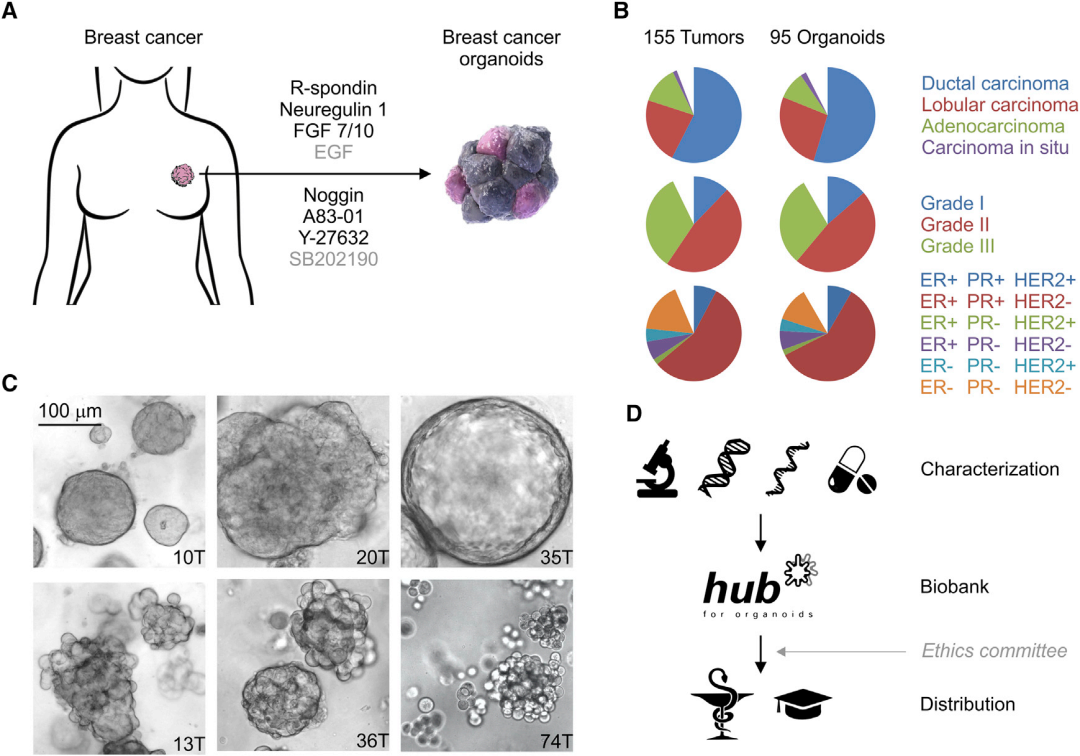
图1. 建立BC类器官生物样本库
02
BC类器官的组织学特征
研究中使用的BC样本和其对应的类器官显示出类似的亚型分布(图1B)。BC类器官的表型与原始BC一致(图2)。例如,导管癌一般产生固体的、连贯的类器官,而小叶癌主要产生盘状的类器官(图2)。80%的HER2阳性和大于90%的HER2阴性BC类器官和原始BC的HER2状态一致(图2)。
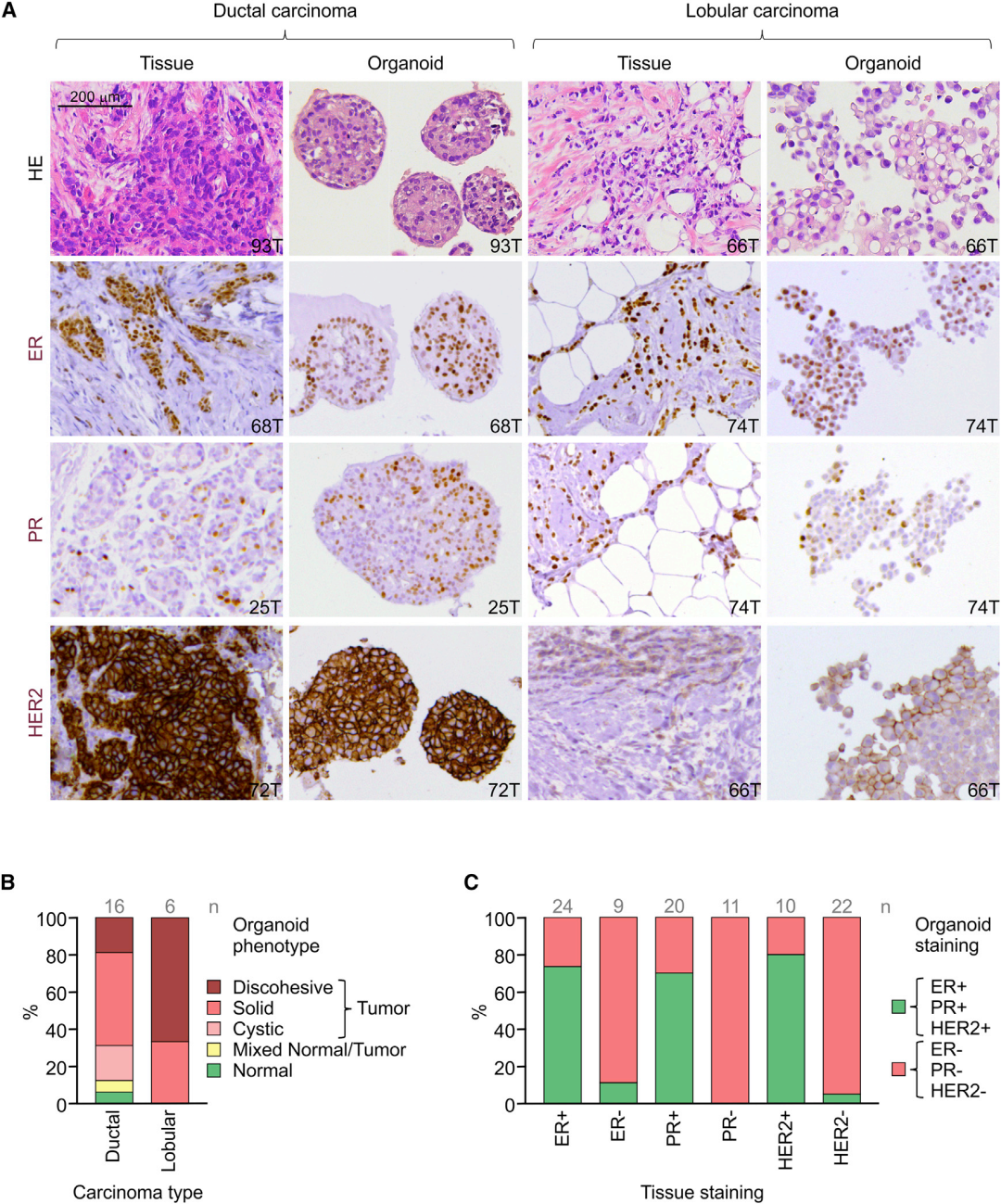
图2. BC类器官的组织学和受体状态
03
BC类器官的基因组特征
作者在BC类器官中发现了BC特征性的染色体数目变化,包括频繁的高倍体和偶尔的低倍体(图3A)。BC类器官保留了原始BC整个基因组的DNA拷贝数的增加和减少(图3B),却比原始BC具有出更明显、低噪音的拷贝数信号。BC类器官再现了癌症基因的原始CNA模式,并且通常显示出更高的信号幅度(图3C),与全基因组的CNAs(图3B)相似。

图3. BC类器官的拷贝数改变
作者用数学方法分析了BCs和类器官中的碱基替换,并绘制了每个患者的每个突变特征的突变总数(图4A)。与患者之间的异质性相反,突变量和突变类型在匹配的BC-类器官对中大部分是相同的(图4A-4C)。
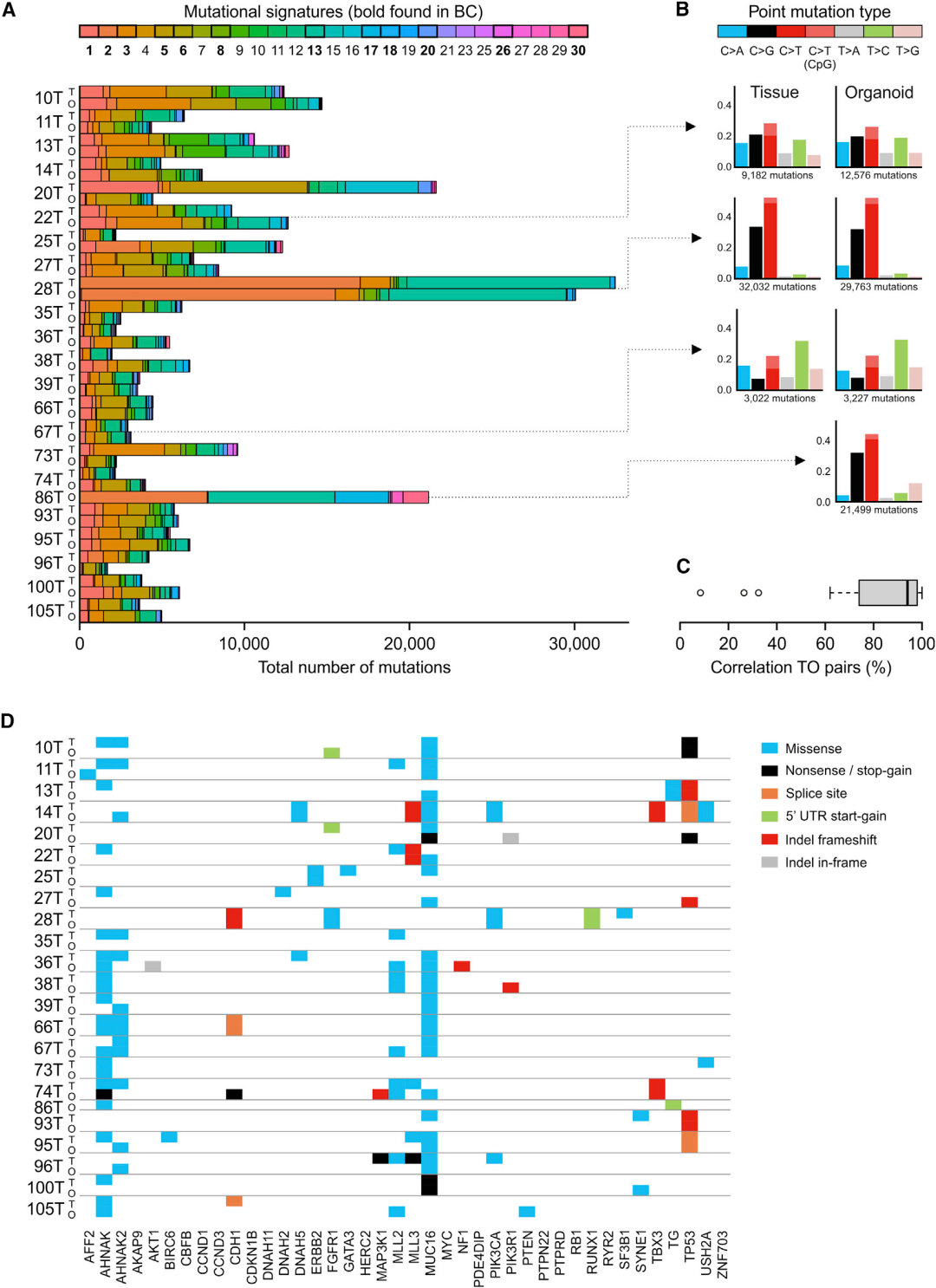
图4. 突变特征和驱动基因分析
04
BC类器官和基因编辑
的基因表达分析
如图5A所示,正常的类器官与五个BC类器官的子集被聚类在一起。当把类器官表达数据与来自TCGA的1100多个BC表达数据结合起来时,作者发现BC类器官可形成所有主要的亚群,并在整个数据集中随机分布(图5B)。

图5. RNA-Seq分析BC类器官的基因表达
05
药物筛选
作者对BC类器官使用了针对HER信号通路的药物(图6A),并进行了细胞活力测定。通过检测每种药物21个浓度获得剂量反应曲线,并确定了各药物的IC50(图6B和6C)。作者发现了几个相对的IC50值,表明存在不同的易感类器官亚群(图6B)。具有高BRCA1/2特征的BC类器官对PARPi敏感,而具有低BRCA1/2特征的BC类器官却不敏感(图6C)。
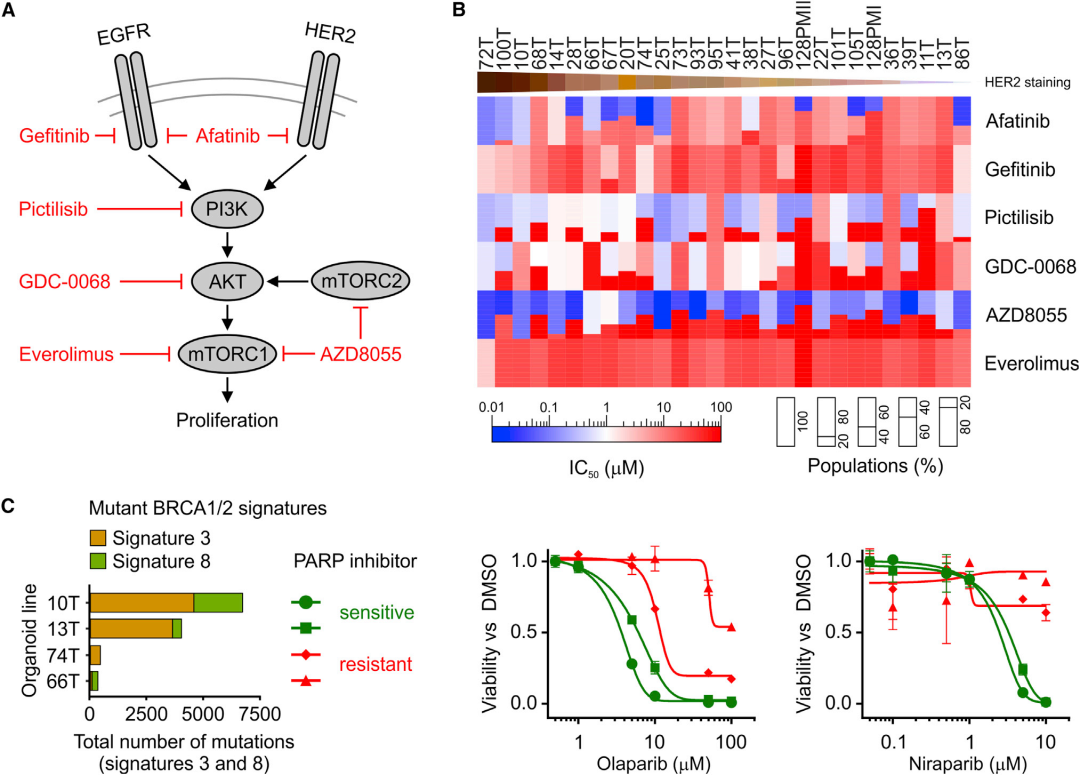
图6. BC类器官允许体外药物筛选
06
与体内药物反应的比较
为了比较体外和体内的药物反应,作者首先选择了两个对体外阻断HER信号的药物有不同反应的BC类器官系(图7A),并将每一系的细胞移植到10只小鼠的双侧。一旦肿瘤生长超过50立方毫米,相应的小鼠将接受10毫克/克体重的阿法替尼或安慰剂治疗28天(图7B)。有阿法替尼抗性的BC类器官系27T,在接受阿法替尼和安慰剂治疗时,肿瘤生长速度几乎相同(图7B)。对阿法替尼敏感的类器官系10T,在接受阿法替尼治疗时的生长速度明显慢于安慰剂组(图7B)。携带27T肿瘤的小鼠需要在同一时间处死,而携带10T肿瘤的小鼠在接受阿法替尼治疗时,与安慰剂相比寿命明显延长(图7B),再现了各自的体外药物反应。BC类器官对他莫西芬的体外反应与各自患者的反应一致(图7C),表明BC类器官有潜力代替体内模型作为药物预测工具。
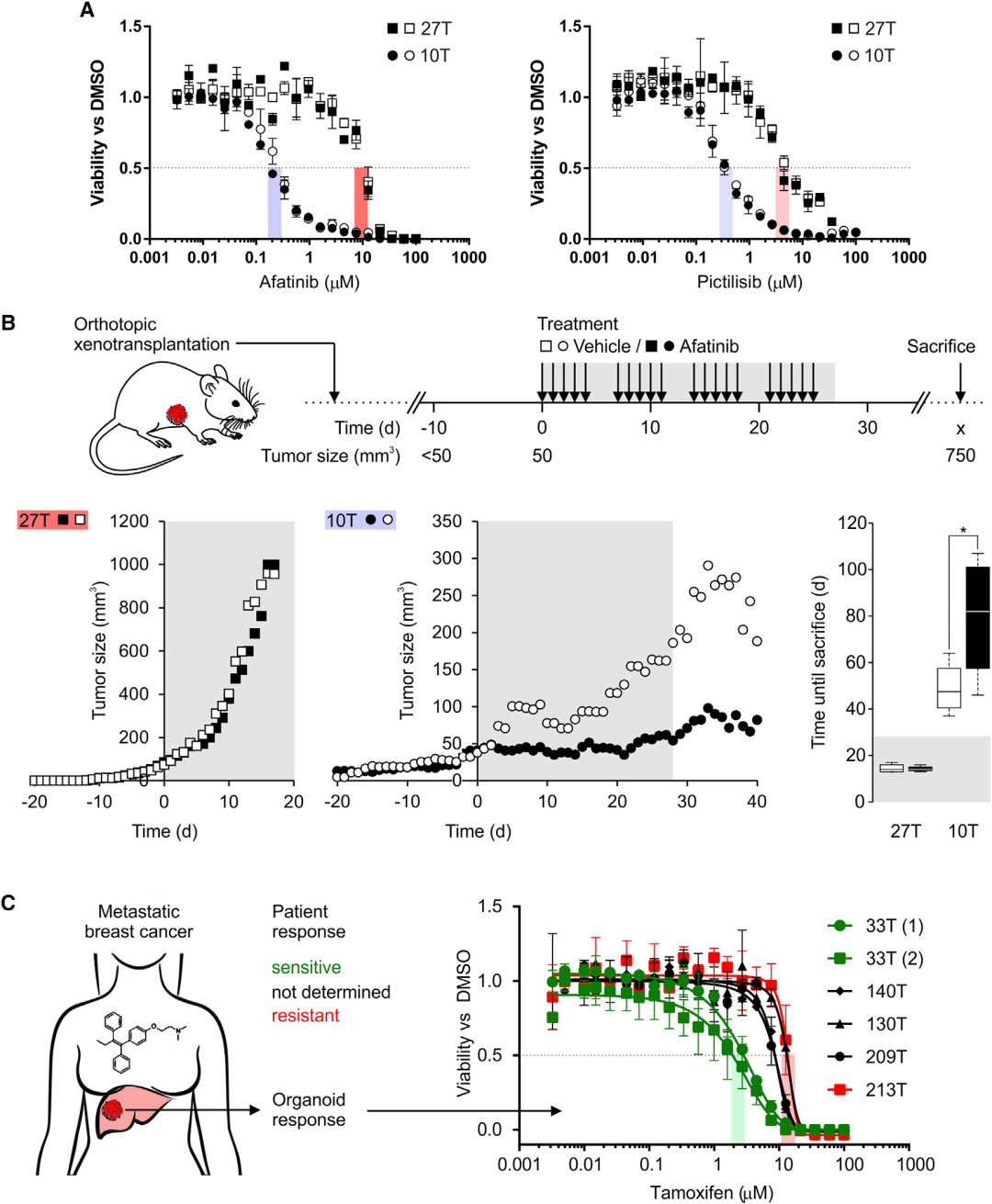
图7. BC类器官再现体内的药物反应
结论
由于BC类器官再现了BC的主要特征,它们可作为体外2D细胞系和体内PDX模型之外的第三个临床前BC模型。BC类器官的表型多样性反映了BC组织学。BC类器官可以进行基因编辑,进而可以进行表型筛选和假设测试。BC类器官还可以从纯肿瘤上皮细胞中提取遗传数据。由于没有''污染''遗传上正常的细胞类型,可以得到更干净的RNA图谱,也更容易检测体细胞突变。在基因表达分析中,BC类器官可以更清楚地显现基于表达的亚型,并找出如上皮细胞黏附的生物问题的原因。然而,体外缺乏的肿瘤微环境可能导致肿瘤-类器官对的表达谱差异。未来的研究可尝试:1)检测所切除的BC肿瘤RNA,进行相应的相关性分析,并剖析肿瘤环境和癌细胞基因表达之间的相互的影响。2)从BC活检中生成类器官,并在临床试验中与相应的患者平行治疗。理想情况下, BC类器官可以帮助识别可能的治疗策略和个别患者的耐药性。3)将组织学、遗传学和/或基因表达数据与BC类器官药物反应相联系,将进一步推动对BC的分子和功能理解。
原文出处:
https://doi.org/10.1016/j.cell.2017.11.010
关于赛箔生物
赛箔生物致力于开发生物3D打印、生物材料、体外检测组织产品、再生器官产品,并且基于相关产品开发精准的检测评价方法及服务。目前已开展数百例肿瘤临床样本的生物3D打印微组织构建,经过大量实验研究及一致性验证,能够构建与患者组织高度一致的肿瘤微组织用于药敏检测,涵盖癌种包括肺癌、结直肠癌、脑胶质瘤、神经母细胞瘤、肝母细胞瘤、膀胱癌等高发癌种、难治肿瘤、儿童肿瘤,成功率>90%,可实现1-2周内完成采样至完成药敏检测流程。


生物3D打印技术,是一项前沿生物制造技术,能够用于制造例如类器官、器官芯片等具有不同尺寸规格、复杂程度的体外3D细胞组织模型。结合与人体组织高度相似的仿生生物材料及患者细胞,可以精确地复制患者肿瘤组织的细胞及细胞外基质特征。通过生物3D打印建立的肿瘤微组织与患者肿瘤组织中突变基因及突变类型保持高度一致。作为一项工程技术,能够更高效率、批量化地建立高重现性、高精度的模型。这些优势都使得生物3D打印技术在肿瘤精准医疗研究和临床应用中具有巨大的潜力。
生物3D打印构建流程
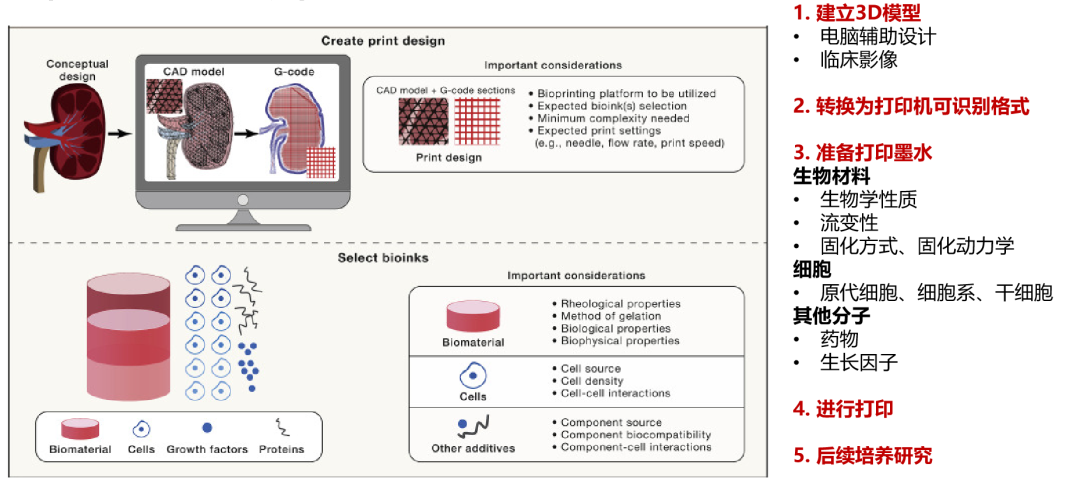
通过生物3D打印建立的肿瘤微组织,可以为患者提供个体化的治疗方案药物敏感性检测,包括类器官可检测的化疗药物、靶向药物。同时,在多种癌种,包括肺癌、结直肠癌等癌种中,生物3D打印为组织中可检测出较高比例免疫细胞,同时由于生物3D打印可以进行不同细胞组合的微组织模型制作,因此也可进行免疫治疗药物的检测,更好地满足患者的需求。
光固化生物3D打印后细胞存活率高、
并维持在体特性
如选择通过生物3D打印技术建立肿瘤微组织,大部分注意事项可参考专家共识针对肿瘤类器官的注意事项,此外运输时间方面相对类器官较为宽裕。目前样本质量、体积达标的情况下,在24小时内送达,均可实现>90%的构建成功率。
生物3D打印作为一种生物制造技术平台即将迭代为一种重要的生命科学工具,利用工程技术构建和模拟人体组织微环境,可涵盖包括类器官、器官芯片等3D模型的制造,从而代替动物实验。在药物研发临床前研究与评价的应用日趋明朗。
✦ ✦✦ ✦✦ ✦✦ ✦
关注我们获取更多咨询

✦ ✦ ✦ ✦ ✦ ✦ ✦ ✦
部分图片文字来自网络,若有侵权,请联系删除。
生物智造创建美好生活
Intelligent Biomanufacturing Creates Better Life
产品
科研服务
走进赛箔
资源中心
联系我们

